heptoses adalah monosakarida memiliki karbon tujuh dan dengan para rumus empiris C 7 H 14 O 7 . Gula ini, seperti monosakarida lainnya, dipolihidroksilasi dan dapat berupa: aldoheptosa, yang memiliki fungsi aldehida pada karbon satu, atau ketoheptosa, yang memiliki gugus keton pada karbon 2.
Heptosa disintesis dalam jalur metabolisme, seperti siklus fotosintesis Calvin dan fase non-oksidatif dari jalur pentosa fosfat. Merupakan penyusun lipo-polisakarida (LPS) pada dinding sel bakteri Gram negatif seperti Escherichia coli , Klebsiella sp., Neisseria sp., Proteus sp., Pseudomonas sp., Salmonella sp., Shigella sp., Dan Vibrio sp.
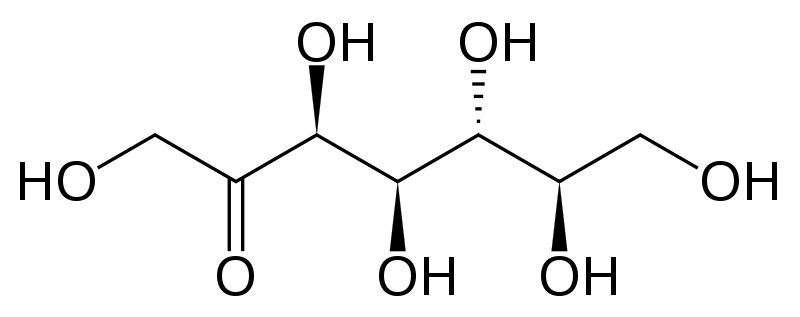
Sumber: Fvasconcellos [Domain publik]
Indeks artikel
Karakteristik
Heptosa, mirip dengan heksosa, ada terutama dalam bentuk sikliknya. Aldoheptosa memiliki lima karbon asimetris dan siklus untuk membentuk piranosa. Sebaliknya, ketoheptosa memiliki empat karbon asimetris, di mana mereka juga membentuk piranosa.
Ketoheptosa alami yang sangat umum pada organisme hidup adalah sedoheptulosa. Gula ini penting dalam pembentukan gula heksosa dalam fotosintesis dan metabolisme karbohidrat pada hewan.
Ketika sedoheptulose dipanaskan dalam encer asam mineral, membentuk campuran mineral kesetimbangan, di mana 80% adalah mengkristal sebagai 2,7-anhydro- β- D-altro-heptulopyranose dan 20% adalah sedoheptulose.
Penentuan kimia heptosa dilakukan dengan asam sulfat dan sistein, difenilamin dan floroglucinol. Dalam kondisi tertentu, adalah mungkin untuk membedakan heptosa dari gula lain. Ia bahkan dapat membedakan antara aldoheptosa dan ketoheptosa.
Banyak aldoheptosa memiliki konfigurasi glisero-D-mannoheptosa. Heptosa, bersama dengan asam gula keto delapan karbon (asam 3-deoksi-D-manno-2-oktulosonat, gula Kdo), adalah komponen struktural LPS, di membran luar lapisan ganda lipid bakteri .
LPS dapat diekstraksi menggunakan 45% fenol dalam campuran air. Kemudian, heptosa dan gula KDO dapat diidentifikasi dengan teknik kolorimetri dan kromatografi.
Pentingnya Biologis Heptosis
Dalam fotosintesis dan jalur pentosa fosfat
Dalam stroma dari kloroplas adalah enzim yang mengkonversi triose fosfat, gliseraldehida-3-fosfat dan dihidroksiaseton fosfat, yang diproduksi oleh asimilasi CO 2 , menjadi tepung. Pembentukan triosa fosfat dan pemulihan karbon, untuk memulai fiksasi CO2 lagi , merupakan dua tahap siklus Calvin.
Selama tahap pemulihan karbon, enzim aldolase bertanggung jawab untuk mengubah eritrosa 4-fosfat (metabolit empat karbon (E4P)) dan dihidroksiketon fosfat (metabolit tiga karbon) menjadi sedoheptulosa 1,7-bifosfat .
Ketoheptosa ini diubah melalui beberapa langkah, dikatalisis secara enzimatik, menjadi ribulosa 1,5-bifosfat.
Ribulosa 1,5-bifosfat adalah metabolit awal dari siklus Calvin. Selain itu, biosintesis sedoheptulosa 7-fosfat (S7P) terjadi di jalur pentosa fosfat, yang merupakan jalur yang ada di semua organisme hidup. Dalam hal ini, aksi transketolase mengubah dua fosfat pentosa menjadi S7P dan gliseraldehida-3-fosfat (GAP).
Kemudian, melalui dua langkah yang dikatalisis oleh transaldolase dan transketolase, S7P dan GAP diubah menjadi fruktosa-6-fosfat dan GAP. Keduanya merupakan metabolit glikolisis.
Dalam lipopolisakarida (LPS) bakteri
Heptosa hadir dalam lipo-polisakarida dan polisakarida dari kapsul bakteri. Motif struktural LPS di enterobacteria terdiri dari lipid A, yang terdiri dari dimer dari 2-amino-2-deoksi-D-glukosa dihubungkan oleh β – (1®6) obligasi. Ini memiliki dua ester fosfat dan kelompok asam lemak rantai panjang.
Lipid A dihubungkan ke daerah pusat oleh jembatan tiga gula Kdo dan asam ketodeoxyoctulosonic, dihubungkan oleh ikatan glikosidik (2®7). Wilayah ini terikat pada L-glisero-D-mannoheptosis heptosa, dengan konfigurasi alfa anomerik. Ada daerah O-antigen.
Motif struktural ini terdapat pada bakteri Gram negatif, seperti Escherichia coli , Klebsiella sp., Yersinia sp., Pseudomonas sp., Salmonella sp., Serta bakteri patogen lainnya.
Ada varian heptosa yang mencakup konfigurasi berbeda dari stereocenter piranosa dalam oligosakarida, serta rantai samping dalam polisakarida. D-glisero-D-manno-heptopyranosil hadir di Yersinia enterocolitica , Coxiella burnetti , Mannheimia haemolitica , Aeromonas hydrophila, dan Vibrio salmonicida .
Heptosa D-glisero-D-manno-heptosa hadir sebagai unit rantai samping di wilayah luar LPS strain Proteus dan Haemophilus influenzae ; dan sebagai rantai pendek oligomer sisi dihubungkan oleh α – (1®3) atau α – (1®2), terkait dengan LPS motif struktural Klebsiella pneumonie .
Pada strain Vibrio cholerae , daerah antigen-O memiliki D-glisero-D-manno-heptosa dengan konfigurasi anomerik (alfa dan beta).
Dalam glikoprotein bakteri
Lapisan permukaannya (lapisan S) terdiri dari subunit protein yang identik, yang menutupinya dalam organisasi dua dimensi. Mereka ditemukan pada bakteri Gram-positif dan Gram-negatif dan archaebacteria. Protein pada lapisan ini memiliki glikopeptida yang memanjang dengan rantai polisakarida.
Glikoprotein dari Aneurinibacillus thermoaerophilus , satu gram bakteri positif, memiliki mengulang unit disakarida ®3) -Dglycero- β -D-mano-Hepp- (1®4) – α -L-Rhap- (1® di lapisan S.
Salah satu fungsi glikoprotein adalah adhesi. Misalnya, ada glikoprotein yang mengukur adhesi sebagai protein autotransporter (AIDA-I) pada galur E. coli . Biosintesis glikoprotein terjadi oleh glikosil transferase, seperti heptosil transferase, yang membutuhkan ADP glisero-manno-heptosa.
Perpaduan
Sintesis kimia dan kombinasi metode kimia dan enzimatik dari heptosa fosfat teraktivasi dan heptosa-nukleotida telah memungkinkan untuk menjelaskan jalur metabolisme yang digunakan mikroorganisme untuk menghasilkan zat ini.
Banyak metode sintesis mempersiapkan manno-heptosa 6-epimerik untuk mensintesis L-glisero-D-manno-heptosa. Metode ini didasarkan pada pemanjangan rantai dari karbon anomerik, atau gugus aldehida, menggunakan pereaksi Grignard. Glikosilasi dilakukan dengan adanya gugus pelindung asil.
Dengan cara ini, ada stereocontrol melestarikan α -anomeric konfigurasi . Tioglikosida anomerik dan turunan trikloroasetimidat berfungsi sebagai donor gugus heptosil. Prosedur yang lebih baru melibatkan pembentukan selektif β -heptosides dan 6-deoksi-heptoside derivatif.
Biosintesis heptosa-nukleotida yang teraktivasi dimulai dari sedoheptulosa 7-fosfat, yang diubah menjadi D-glisero-D-manno-heptosa 7-fosfat. Sebuah fosfomutase telah diusulkan untuk membentuk heptosil fosfat anomerik. Kemudian, transferase heptosil mengkatalisis pembentukan ADP D-glisero-D-manno-heptosa.
Akhirnya, epimerase mengubah konfigurasi ADP D-glisero-D-manno-heptosa menjadi ADP L-glisero-D-manno-heptosa.
Selain itu, studi kimia telah dilakukan untuk memahami mekanisme di mana enzim ini melakukan katalisis. Misalnya, mereka menggunakan benzil mannopiranosida terbenzilasi, yang dioksidasi menjadi turunan manouronik.
Pengobatan dengan asam klorida mengubah turunan manouronic menjadi diazoketon. Pengobatan dengan diazobenzil fosfat menghasilkan campuran L-glisero-7-fosfat dan D-glisero-7-fosfat.
Referensi
- Collins, PM 2006. Kamus karbohidrat dengan CD-ROM. Chapman & Hall / CRC, Boca Raton.
- Cui, SW 2005. Karbohidrat makanan: kimia, sifat fisik, dan aplikasi. CRC Press, Boca Raton.
- Ferrier, RJ 2000. Kimia karbohidrat: monosakarida, disakarida dan oligosakarida spesifik. Royal Society of Chemistry, Cambridge.
- Hofstad, T. 1974. Distribusi heptosa dan 2-keto-3-deoxy-octonate di Bacteroidaceae. Jurnal Mikrobiologi Umum, 85, 314–320
- Kosma, P. 2008. Terjadinya, sintesis dan biosintesis heptosis bakteri. Kimia Organik Saat Ini, 12, 1021-1039.
- Nelson, DL, Cox, MM 2017. Prinsip-prinsip biokimia Lehninger. WH Freeman, New York.
- Pigman, W. 1957. Karbohidrat: kimia, biokimia, fisiologi. Pers Akademik, New York.
- Pigman, W., Horton, D. 1970. Karbohidrat: kimia dan biokimia. Pers Akademik, New York.
- Sinnott, ML 2007. Struktur dan mekanisme kimia karbohidrat dan biokimia. Royal Society of Chemistry, Cambridge.
- Stick, RV, Williams, SJ 2009. Karbohidrat: molekul penting kehidupan. Elsevier, Amsterdam.
- Voet, D., Voet, JG, Pratt, CW 2008. Dasar-dasar biokimia – kehidupan di tingkat molekuler. Wiley, Hoboken.

