elektroforesis adalah teknik yang digunakan untuk memisahkan molekul-molekul dalam medan listrik. Ini ada hubungannya, khususnya, dengan migrasi partikel bermuatan di bawah pengaruh arus listrik yang diterapkan antara dua kutub, satu positif dan yang lain negatif.
Saat ini elektroforesis mungkin merupakan salah satu prosedur paling rutin yang dilakukan selama pengembangan eksperimen, terutama di bidang yang berkaitan dengan kimia analitik, biokimia, dan ilmu biologi dan kedokteran pada umumnya.

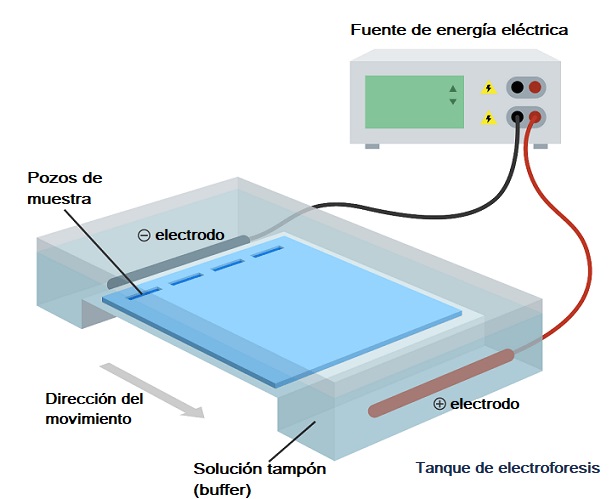
Sel untuk elektroforesis. Sumber: Melodygar / CC BY-SA (https://creativecommons.org/licenses/by-sa/4.0)
Ini digunakan untuk memisahkan protein, peptida, DNA , RNA dan molekul lain sesuai dengan muatan, ukuran, kepadatan dan kemurniannya.
Rumah komersial yang berbeda telah merancang format yang berbeda, dengan aplikasi yang berbeda dan utilitas yang sesuai untuk tujuan tertentu, namun, semua prosedur memerlukan unsur dasar yang sama:
– Sumber energi untuk menghasilkan muatan listrik
– Sarana pendukung untuk terjadinya perpisahan
– Larutan penyangga ( buffer ) untuk menjaga pH tetap konstan
Indeks artikel
Dasar
Elektroforesis tidak lebih dari migrasi (pemisahan) partikel atau molekul bermuatan (alami atau buatan) dalam media atau penyangga di bawah pengaruh medan listrik.
Teknik ini didasarkan pada salah satu persamaan fisika utama elektromagnetisme, yang menyatakan bahwa gaya sama dengan muatan listrik dikalikan dengan medan listrik yang diterapkan pada titik tersebut (F (gaya) = q (muatan listrik) x E (medan listrik) )).
Menurut persamaan ini, dua partikel dengan massa yang sama, tetapi berbeda muatan, akan bergerak dengan laju yang berbeda dalam medan listrik yang sama. Selanjutnya, kecepatan pergerakan partikel-partikel ini akan bergantung pada hubungan antara muatan dan massanya.
Para ilmuwan telah memanfaatkan sifat dan hubungan muatan / massa ini untuk memisahkan komponen biomolekul menjadi bagian terkecilnya, serta untuk memisahkan molekul yang berbeda dalam campuran, di antara aplikasi lainnya.
Penting untuk diingat bahwa molekul biologis seperti asam amino, peptida, protein, beberapa karbohidrat, nukleotida, dan asam nukleat semuanya memiliki sesuatu yang kita sebut “gugus yang dapat terionisasi,” itulah sebabnya mereka dapat eksis sebagai spesies bermuatan positif atau negatif dalam kondisi tertentu. .pH.
Teknik
Meskipun ada beberapa jenis elektroforesis, elektroforesis gel adalah yang paling banyak digunakan dalam analisis biokimia, biologi molekuler, dan bioteknologi, jadi inilah yang akan kita bicarakan secara singkat dalam istilah teknis.
Seperti namanya, elektroforesis gel melibatkan penggunaan media pendukung padat dalam bentuk gel, baik untuk analisis / pemisahan campuran protein atau asam nukleat (DNA dan / atau RNA) di bawah pengaruh medan listrik.
Sistem atau peralatan yang digunakan untuk melakukan “lari” elektroforesis gel dapat berbentuk horizontal (umumnya digunakan untuk asam nukleat) atau vertikal (umumnya digunakan untuk protein).
– Contoh teknik elektroforesis asam nukleat
Asam nukleat biasanya dipisahkan menggunakan gel agarosa (polisakarida galaktosa) yang disiapkan dengan larutan buffer yang sesuai (Tris / Asetat / EDTA atau Tris / Borat / EDTA) dan konsentrasinya akan menentukan “resolusi” fragmen dengan ukuran berbeda.
Persiapan sampel
Langkah pertama sebelum melakukan elektroforesis pada gel agarosa adalah mendapatkan sampel. Ini akan tergantung pada tujuan percobaan dan sampel dapat berupa produk pencernaan enzimatik, reaksi berantai polimerase (PCR), pemurnian asam nukleat, dll.
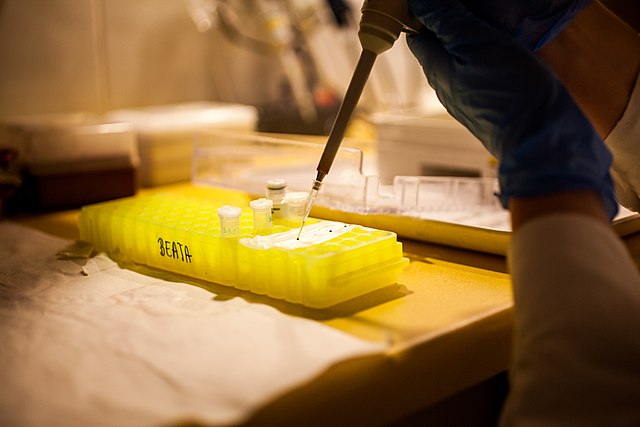
Mencampur sampel dengan buffer pemuatan (Sumber: Karolina Fok / CC BY (https://creativecommons.org/licenses/by/4.0) melalui Wikimedia Commons)
Setelah diperoleh, itu dicampur dengan larutan berwarna (larutan pemuatan) yang memungkinkan pengendapan sampel dengan cepat di dalam sumur, karena memiliki gliserol dan pewarna yang memungkinkan proses diikuti secara visual.
Persiapan gel
Langkah ini terdiri dari pencampuran substrat pembentuk gel (agarosa) dalam jumlah yang diperlukan dengan larutan buffer, melelehkannya menggunakan panas dan memadatkannya pada penyangga yang berfungsi sebagai “cetakan”.
Selama pembuatan gel, “sisir” dimasukkan ke dalam gel yang ditempatkan di “cetakan” untuk membatasi “sumur” tempat sampel akan dimasukkan sebelum dijalankan.
Setelah gel mendingin dan memadat, “sisir” dikeluarkan dan dimasukkan ke dalam wadah yang dikenal sebagai “ember”, yang diisi dengan larutan buffer yang mengalir, (Tris / Asetat / EDTA atau Tris / Borat / EDTA) .
Kuvet ini, pada gilirannya, termasuk dalam apa yang disebut “ruang elektroforesis”, yang tidak lebih dari wadah yang dilalui medan listrik dan yang memiliki ruang di mana gel dimasukkan dan dua bagian yang diisi dengan buffer. solusi ( jalankan buffer ).
Ruang ini memiliki dua elektroda, satu positif dan lainnya negatif, di antaranya pergerakan ion terjadi setelah penerapan medan listrik (terhubung ke sumber listrik).
Pemuatan sampel
Setelah sampel dicampur dengan masing-masing larutan pemuatan, sampel dimasukkan ke dalam “sumur” yang sebelumnya dibuat dalam gel.
Karena asam nukleat memiliki muatan negatif bersih, asam nukleat bermigrasi dari kutub negatif ke kutub positif, jadi ini harus diperhitungkan saat menghubungkan kamera ke sumber listrik, memastikan kutub negatif sesuai dengan situs yang paling umum. ke tempat di mana sampel dimuat.
Waktu berjalan ditetapkan dengan ketergantungan yang ketat pada peneliti yang bertanggung jawab atas eksperimen. Tegangan umumnya dihitung dalam rasio 5 volt untuk setiap sentimeter jarak dalam gel yang memisahkan dua elektroda.
Menampilkan
Ketika proses selesai gel (ketika sampel telah melakukan perjalanan gel dari satu ujung ke ujung lainnya) gel direndam dalam larutan etidium bromida (EtBr), pewarna yang diapit di antara basa nitrogen dan yang “menandai” mereka . , sehingga dapat divisualisasikan dalam transilluminator menggunakan sinar ultraviolet.
Untuk apa elektroforesis?
Elektroforesis secara historis telah digunakan untuk berbagai tujuan. Hari ini, bagaimanapun, kegunaannya sangat tergantung pada “pertanyaan” yang ditanyakan peneliti pada dirinya sendiri dalam kaitannya dengan fenomena atau sistem tertentu, serta jenis elektroforesis yang ingin digunakannya.
Namun, kita dapat membuat daftar beberapa fungsi utama yang dimiliki teknik ini, dimulai dengan yang paling “langka” dan diakhiri dengan yang paling populer dan paling dieksploitasi di dunia ilmu biologi. Elektroforesis berguna:
– Untuk analisis kuantitatif campuran kompleks makromolekul dan untuk perhitungan potensi “zeta” (sifat koloid partikel dalam media cair di bawah pengaruh medan listrik statis).
– Untuk analisis serum darah untuk tujuan diagnostik.
– Untuk pemisahan glikoprotein darah, lipoprotein dan hemoglobin.
– Untuk analisis makanan, produk farmasi dan polutan lingkungan.
Elektroforesis dalam gel agarosa
– Untuk pemisahan fragmen DNA setelah pencernaannya dengan enzim restriksi.
– Untuk pemisahan molekul asam nukleat sebelum dipindahkan ke membran untuk analisis selanjutnya.
– Untuk analisis produk PCR (polymerase chain reaction) untuk memverifikasi apakah terjadi amplifikasi atau tidak.
– Untuk memperkirakan ukuran molekul dalam campuran DNA atau RNA.
– Mengestimasi jumlah dan/atau kualitas asam nukleat yang dimurnikan.
Elektroforesis pada gel poliakrilamida dalam kondisi denaturasi atau asli
– Untuk menentukan ukuran protein.
– Untuk mengidentifikasi protein.
– Untuk menentukan kemurnian sampel setelah beberapa langkah pemurnian.
– Untuk mengidentifikasi adanya ikatan disulfida intramolekul.
– Untuk mengetahui interaksi antar protein.
– Menentukan titik isoelektrik suatu protein.
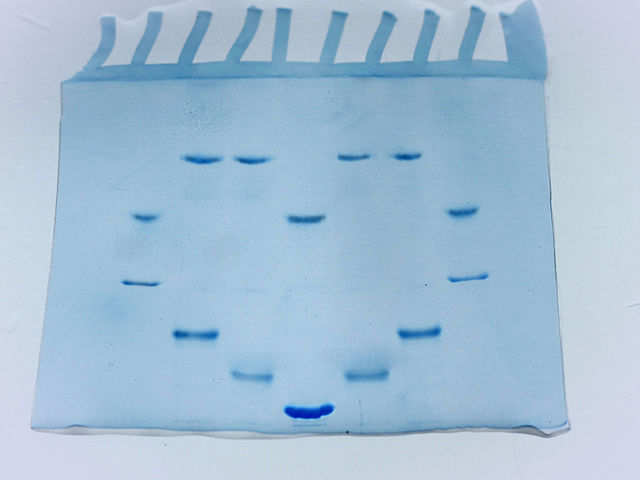
Foto gel akrilamida setelah menjalankan beberapa sampel protein (Sumber: Larionova.marina / CC BY-SA (https://creativecommons.org/licenses/by-sa/4.0) melalui Wikimedia Commons)
Faktor-Faktor yang Mempengaruhi Elektroforesis
Migrasi suatu partikel dalam medan listrik tergantung pada berbagai faktor, di antaranya adalah:
– Muatan listriknya
– Ukuran molekulnya
– Hidrofobisitas dan bentuknya
– Besarnya medan listrik yang diterapkan padanya
– Suhu sistem dan kekuatan ion dari larutan buffer yang digunakan
– Sifat lingkungan tempat ia berada
Sehubungan dengan sampel
Di antara parameter yang terkait dengan partikel (sampel) yang dikenai medan listrik, faktor utama yang mempengaruhi proses ini berkaitan dengan muatan, ukuran, dan bentuknya.
Semakin tinggi muatan bersih pada suatu partikel, semakin tinggi laju migrasinya dan besarnya ini akan tergantung pada pH. Namun, hubungan dengan ukuran berbanding terbalik, yang berarti bahwa semakin “besar” molekul, semakin lambat ia akan bermigrasi.
Sehubungan dengan medan listrik
Sejauh ini kita telah berbicara tentang pentingnya medan listrik untuk mencapai pergerakan partikel dengan elektroforesis, tetapi kita belum mendefinisikan apa itu: gaya listrik per satuan muatan atau, dalam istilah yang lebih sederhana, wilayah ruang di mana terdapat kekuatan listrik.
Parameter mengenai medan listrik yang dapat mempengaruhi migrasi adalah tegangan, arus dan hambatan.
Tegangan mempengaruhi “waktu terbang” molekul yang terpisah setelah menerapkan medan listrik. Semakin tinggi, semakin cepat mereka bergerak.
Arus (aliran elektron yang kontinu dan seragam yang “didorong” oleh sumber tegangan) dilakukan antara elektroda sistem elektroforesis berkat ion yang ada dalam larutan buffer. Ini berhubungan langsung dengan tegangan.
Relatif terhadap larutan penyangga
Komposisi, kekuatan ionik, dan pH larutan buffer adalah parameter utama yang mempengaruhi “jalan” elektroforesis, karena mereka secara langsung mempengaruhi beberapa sifat sampel, terutama muatan listrik.
Mengapa? Larutan buffer menstabilkan pH media pendukung di mana elektroforesis terjadi. Komposisinya dapat mempengaruhi perpindahan partikel yang bermigrasi dan juga konsentrasi ion, karena berhubungan langsung dengan arus.
Sehubungan dengan media dukungan
Berbagai jenis dan format elektroforesis juga memiliki media pendukung yang berbeda di mana migrasi terjadi dan di mana ia dapat “direkam” nanti.
Laju migrasi molekul yang dikenai elektroforesis tergantung pada jenis media pendukung, yang biasanya harus inert.
Karakteristik penyerapannya, elektroendo-osmosis (kapasitas pergerakan cairan melalui membran di bawah pengaruh medan listrik) dan kapasitas penyaringan molekuler adalah penting.
Contoh penggunaan elektroforesis
Contoh klasik teknik elektroforesis yang digunakan dalam biologi dan bioteknologi meliputi:
– Elektroforesis dalam gel agarosa (dari bahasa Inggris Agarose Gel Electrophoresis )
– Elektroforesis dalam gel akrilamida dalam kondisi denaturasi (SDS-PAGE, Elektroforesis Gel Sodium Dodecyl Sulphate Polyacrylamide )
– Elektroforesis dalam gel akrilamida dalam kondisi asli (BN-PAGE, Elektroforesis Gel Poliakrilamida Asli Biru )
– Elektroforesis Dua Dimensi (2D-PAGE, Elektroforesis Gel Poliakrilamida Dua Dimensi )
– Elektroforesis Kapiler ( Elektroforesis Kapiler )
– Pemfokusan Isoelektro ( Isoelektrofokus )
– Medan pulsa elektroforesis (dari English Pulsed Field Electrophoresis )
Referensi
- Beck, Kevin. (2020, 25 Mei). Jenis-Jenis Elektroforesis. Sains.com. Diperoleh dari sciencing.com
- Esai, Inggris. (November 2018). Jenis dan Kegunaan Elektroforesis. Diperoleh dari ukessays.com
- Nelson, DL, Lehninger, AL, & Cox, MM (2008). Prinsip biokimia Lehninger. Macmillan.
- Parmar, P. (Agustus 2018). Elektroforesis: Arti, Definisi dan Klasifikasi (Dengan Diagram). Teknologi Bio. Diperoleh dari biotechnologynotes.com
- Perrett, D. (2010). 200 tahun Elektroforesis. kromatografi. Hari ini, 4-7.
- Rightti, PG (2005). Elektroforesis: pawai sen, pawai sepeser pun. Jurnal Kromatografi A, 1079 (1-2), 24-40.
- Rilbe, H. (1995). Beberapa kenangan tentang sejarah elektroforesis. Elektroforesis, 16 (1), 1354-1359.
- Vesterberg, O. (1993). Sejarah singkat metode elektroforesis. Elektroforesis, 14 (1), 1243-1249.
- Vinayagam, M. (Tanpa Tanggal). Faktor yang mempengaruhi elektroforesis. akademi.edu. Diperoleh dari academia.edu

