serin adalah salah satu dari 22 asam amino dasar, meskipun ini tidak diklasifikasikan sebagai asam amino esensial bagi manusia dan hewan lainnya, karena disintesis oleh tubuh manusia.
Menurut tata nama tiga huruf, serin digambarkan dalam literatur sebagai Ser (S dalam kode satu huruf). Asam amino ini berpartisipasi dalam sejumlah besar jalur metabolisme dan memiliki karakteristik polar, tetapi tidak memiliki muatan pada pH netral.
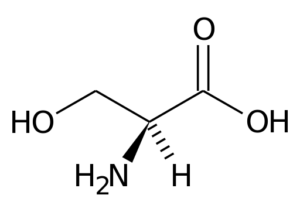
Representasi struktur asam amino Serine (Sumber: Paginazero di it.wikipedia [Domain publik] melalui Wikimedia Commons)
Banyak enzim yang penting bagi sel memiliki konsentrasi residu serin yang melimpah di tempat aktifnya, itulah sebabnya asam amino ini memiliki banyak implikasi fisiologis dan metabolik.
Serin, di antara banyak fungsinya, berpartisipasi sebagai molekul prekursor dan perancah dalam biosintesis asam amino lain seperti glisin dan sistein dan merupakan bagian dari struktur sphingolipid yang ada dalam membran sel.
Tingkat sintesis serin bervariasi di setiap organ dan, di samping itu, berubah sesuai dengan tahap perkembangan di mana individu tersebut berada.
Para ilmuwan telah mengusulkan bahwa konsentrasi L-serin dalam jaringan otak meningkat seiring bertambahnya usia, karena permeabilitas penghalang darah-otak menurun di otak orang dewasa, yang dapat menyebabkan gangguan otak yang parah.
L-serin diketahui penting untuk biosintesis neurotransmiter, fosfolipid, dan makromolekul kompleks lainnya, karena menyediakan prekursor untuk berbagai jalur metabolisme ini.
Berbagai penelitian telah menunjukkan bahwa memasok suplemen L-serin atau konsentrat untuk jenis pasien tertentu meningkatkan homeostasis glukosa, fungsi mitokondria, dan mengurangi kematian neuron.
Indeks artikel
Karakteristik dan struktur
Semua asam amino sebagai struktur dasarnya memiliki gugus karboksil dan gugus amino yang terikat pada atom karbon yang sama; Namun, ini berbeda satu sama lain dengan rantai sampingnya, yang dikenal sebagai gugus R, yang dapat bervariasi dalam ukuran, struktur, dan bahkan muatan listriknya.
Serin mengandung tiga atom karbon: karbon pusat terikat, di satu sisi, ke gugus karboksil (COOH) dan di sisi lain, ke gugus amino (NH3 +). Dua ikatan karbon pusat lainnya ditempati oleh atom hidrogen dan oleh gugus CH2OH (gugus R), karakteristik serin.
Karbon pusat yang mengikat gugus amino dan karboksil dari asam amino dikenal sebagai karbon-. Atom karbon lain dalam kelompok R ditunjuk oleh huruf-huruf alfabet Yunani.
Dalam kasus serin, misalnya, satu-satunya atom karbon dalam gugus R-nya, yang terikat pada gugus OH, dikenal sebagai -karbon.
Klasifikasi
Serin diklasifikasikan dalam kelompok asam amino polar tidak bermuatan. Anggota kelompok ini adalah asam amino yang sangat larut dalam air, yaitu senyawa hidrofilik. Dalam serin dan treonin, hidrofilisitas disebabkan oleh kemampuannya untuk membentuk ikatan hidrogen dengan air melalui gugus hidroksil (OH).
Dalam kelompok asam amino polar yang tidak bermuatan, sistein, asparagin, dan glutamin juga dikelompokkan. Semua ini memiliki gugus polar dalam rantai R mereka, namun, gugus ini tidak dapat terionisasi dan pada pH mendekati netral mereka membatalkan muatannya, menghasilkan senyawa dalam bentuk ” zwitterion “.
Stereokimia
Asimetri umum asam amino membuat stereokimia senyawa ini sangat penting dalam jalur metabolisme di mana mereka berpartisipasi. Dalam kasus serin, dapat ditemukan sebagai D- atau L-serin, yang terakhir disintesis secara eksklusif oleh sel-sel sistem saraf yang dikenal sebagai astrosit.
Karbon dari asam amino adalah karbon kiral, karena mereka memiliki empat substituen berbeda yang terikat, yang menghasilkan bahwa setidaknya ada dua stereoisomer yang dapat dibedakan untuk setiap asam amino.
Stereoisomer adalah bayangan cermin dari suatu molekul, yaitu, yang satu tidak dapat ditumpangkan pada yang lain. Mereka dilambangkan dengan huruf D atau L karena secara eksperimental larutan asam amino ini memutar bidang cahaya terpolarisasi ke arah yang berlawanan.
L-serin yang disintesis dalam sel sistem saraf berfungsi sebagai substrat untuk mensintesis glisin atau D-serin. D-serin adalah salah satu unsur yang paling penting untuk pertukaran vesikel antara neuron terjadi, itulah sebabnya beberapa penulis mengusulkan bahwa kedua isoform serin, pada kenyataannya, asam amino esensial untuk neuron.
Fitur
Gugus OH serin dalam rantai R membuatnya menjadi nukleofil yang baik, sehingga merupakan kunci aktivitas banyak enzim dengan serin pada situs aktifnya. Serin adalah salah satu substrat yang diperlukan untuk sintesis nukleotida NADPH dan glutathione.
L-serin sangat penting untuk pengembangan dan berfungsinya sistem saraf pusat . Penelitian telah menunjukkan bahwa pengiriman eksogen L-serin dosis rendah ke neuron hipokampus dan sel Purkinje in vitro meningkatkan kelangsungan hidup mereka.
Berbagai penelitian sel kanker dan limfosit telah menemukan bahwa unit karbon yang bergantung pada serin diperlukan untuk produksi nukleotida yang berlebihan, serta proliferasi sel kanker selanjutnya.
Selenocysteine adalah salah satu dari 22 asam amino dasar dan diperoleh semata-mata sebagai turunan serin. Asam amino ini hanya diamati pada beberapa protein, mengandung selenium bukannya belerang yang terikat pada sistein dan disintesis mulai dari serin yang diesterifikasi.
Biosintesis
Serin adalah asam amino non-esensial, karena disintesis oleh tubuh manusia. Namun, ini dapat diasimilasi dari makanan sumber yang berbeda seperti protein dan fosfolipid, terutama.
Serin disintesis dalam bentuk L-nya melalui konversi molekul glisin, suatu reaksi yang dimediasi oleh enzim hidroksimetil-transferase.
Diketahui bahwa situs utama sintesis L-serin adalah di astrosit dan bukan di neuron. Dalam sel-sel ini, sintesis terjadi melalui jalur fosforilasi di mana 3-fosfogliserat, zat antara glikolitik, berpartisipasi.
Tiga enzim bekerja dalam jalur ini: 3-fosfogliserat dehidrogenase, fosfoserin-transferase dan fosfoserin-fosfatase.
Organ penting lainnya dalam hal sintesis serin adalah hati, ginjal , testis, dan limpa. Enzim yang mensintesis serin melalui jalur selain fosforilasi hanya ditemukan di hati dan ginjal.
Salah satu rute sintesis serin pertama yang diketahui adalah jalur katabolik yang terlibat dalam glukoneogenesis, di mana L-serin diperoleh sebagai metabolit sekunder. Namun, kontribusi rute ini terhadap produksi serin tubuh rendah.
Metabolisme
Saat ini diketahui bahwa serin dapat diperoleh dari metabolisme karbohidrat di hati, di mana asam D-gliserat, asam 3-fosfogliserat dan asam 3-fosfohidroksipiruvat diproduksi. Berkat proses transaminasi antara asam 3-hidroksi piruvat dan alanin, serin diproduksi.
Eksperimen yang dilakukan dengan tikus yang secara radioaktif melabeli karbon 4 dari glukosa, telah menyimpulkan bahwa karbon ini secara efektif dimasukkan ke dalam kerangka karbon serin, menunjukkan bahwa asam amino tersebut memiliki prekursor tiga karbon yang kemungkinan berasal dari piruvat.
Pada bakteri, enzim L-serin-deaminase adalah enzim utama yang bertugas memetabolisme serin: ia mengubah L-serin menjadi piruvat. Enzim ini diketahui hadir dan aktif dalam kultur E. coli yang ditumbuhkan dalam media minimal dengan glukosa.
Tidak diketahui secara pasti apa fungsi sebenarnya dari L-serin-deaminase dalam mikroorganisme ini, karena ekspresinya diinduksi oleh efektor mutasi yang merusak DNA oleh radiasi ultraviolet, dengan adanya asam nalidiksat, mitomisin dan lain-lain. berikut bahwa itu harus memiliki implikasi fisiologis yang penting.
Makanan yang kaya akan serin
Semua makanan dengan konsentrasi tinggi protein kaya akan serin, terutama telur, daging dan ikan. Namun, ini adalah asam amino non-esensial, jadi tidak perlu menelannya, karena tubuh mampu mensintesisnya sendiri.
Beberapa orang menderita kelainan langka, karena mereka memiliki fenotipe dengan defisiensi mekanisme sintesis serin dan glisin, oleh karena itu, mereka perlu mengonsumsi suplemen makanan pekat untuk kedua asam amino.
Selain itu, merek komersial yang mengkhususkan diri dalam penjualan suplemen vitamin (Lamberts, Now Sport, dan HoloMega) menawarkan konsentrat fosfatidilserin dan L-serin untuk meningkatkan produksi massa otot pada atlet dan angkat besi yang sangat kompetitif.
Penyakit terkait
Kerusakan enzim yang terlibat dalam biosintesis serin dapat menyebabkan patologi yang serius. Penurunan konsentrasi serin dalam plasma darah dan cairan serebrospinal dapat menyebabkan hipertonia, retardasi psikomotor, mikrosefali, epilepsi, dan gangguan kompleks susunan saraf pusat.
Saat ini, telah ditemukan bahwa defisiensi serin terlibat dalam perkembangan diabetes mellitus, karena L-serin diperlukan untuk sintesis insulin dan reseptornya.
Bayi dengan cacat pada biosintesis serin secara neurologis abnormal saat lahir, dengan retardasi pertumbuhan intrauterin, mikrosefali kongenital, katarak, kejang, dan keterlambatan perkembangan saraf yang parah.
Referensi
- Elsila, JE, Dworkin, JP, Bernstein, MP, Martin, MP, & Sandford, SA (2007). Mekanisme pembentukan asam amino dalam analog es antarbintang. Jurnal Astrofisika, 660 (1), 911.
- Ichord, RN, & Bearden, DR (2017). Ensefalopati metabolik perinatal. Dalam Neurologi Pediatrik Swaiman (hlm. 171-177). lain.
- Mothet, JP, Induk, AT, Wolosker, H., Brady, RO, Linden, DJ, Ferris, CD, … & Snyder, SH (2000). D-serin adalah ligan endogen untuk situs glisin dari reseptor N-metil-D-aspartat. Prosiding National Academy of Sciences, 97 (9), 4926-4931
- Nelson, DL, Lehninger, AL, & Cox, MM (2008). Prinsip biokimia Lehninger. Macmillan.
- Rodríguez, AE, Ducker, GS, Billingham, LK, Martinez, CA, Mainolfi, N., Suri, V.,… & Chandel, NS (2019). Metabolisme Serin Mendukung Produksi Makrofag IL-1β. Metabolisme sel, 29 (4), 1003-1011.
- Tabatabaie, L., Klomp, LW, Berger, R., & De Koning, TJ (2010). Sintesis L-serin dalam sistem saraf pusat: ulasan tentang gangguan defisiensi serin. Genetika molekuler dan metabolisme, 99 (3), 256-262.

