triptofan (Trp, W) adalah asam amino diklasifikasikan dalam kelompok asam amino esensial karena tubuh manusia tidak dapat mensintesis dan harus mendapatkan itu melalui diet.
Beberapa makanan seperti susu dan turunannya, daging, telur dan beberapa sereal seperti quinoa dan kedelai mengandung asam amino esensial dan, oleh karena itu, merupakan sumber triptofan yang penting.
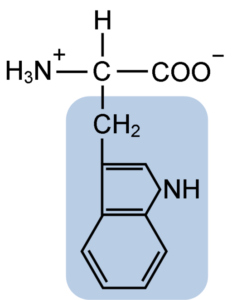
Struktur kimia asam amino Triptofan (Sumber: Clavecin [CC BY-SA 4.0 (https://creativecommons.org/licenses/by-sa/4.0)] melalui Wikimedia Commons)
Di alam, lebih dari 300 asam amino yang berbeda diketahui dan hanya 22 di antaranya yang merupakan unit monomer protein seluler. Di antara yang terakhir, 9 adalah asam amino esensial, termasuk triptofan, namun esensi masing-masing berbeda dari satu spesies ke spesies lainnya.
Triptofan memiliki berbagai fungsi, termasuk partisipasinya dalam sintesis protein, dalam sintesis serotonin, yang merupakan vasokonstriktor dan neurotransmitter yang kuat, melatonin dan dalam sintesis kofaktor NAD.
Di kingdom tumbuhan, triptofan adalah prekursor mendasar dari hormon tanaman auksin (asam indole-3-asetat). Ini dapat disintesis oleh beberapa bakteri seperti E. coli dari chorismate, yang dihasilkan dari beberapa turunan glikolitik seperti phosphoenolpyruvate dan erythrose-4-phosphate.
Degradasi pada mamalia terjadi di hati, di mana ia digunakan untuk sintesis asetil koenzim A (asetil-KoA), dan untuk alasan ini digambarkan sebagai asam amino yang disebut glukogenik, karena dapat memasuki siklus pembentukan glukosa.
Berbagai penelitian telah dilaporkan dengan hasil kontroversial terkait dengan penggunaan triptofan sebagai suplemen makanan untuk pengobatan beberapa patologi seperti depresi dan beberapa gangguan tidur antara lain.
Ada beberapa penyakit yang berhubungan dengan cacat lahir pada metabolisme asam amino. Dalam kasus triptofan, penyakit Hartnup dapat dinamai, karena kekurangan triptofan-2,3-monooksigenase, penyakit keturunan resesif yang ditandai dengan keterbelakangan mental dan kelainan kulit seperti pellagra.
Indeks artikel
Karakteristik
Bersama dengan fenilalanin dan tirosin, triptofan termasuk dalam kelompok asam amino aromatik dan hidrofobik.
Namun, triptofan dicirikan sebagai asam amino yang sedikit hidrofobik karena rantai samping aromatiknya, yang memiliki gugus polar, melemahkan hidrofobisitas ini.
Karena mereka memiliki cincin terkonjugasi, mereka memiliki penyerapan cahaya yang kuat di wilayah spektrum dekat ultraviolet dan karakteristik ini sering digunakan untuk analisis struktural protein.
Ini menyerap sinar ultraviolet (antara 250 dan 290 nm) dan, meskipun asam amino ini tidak terlalu banyak dalam struktur sebagian besar protein dalam tubuh manusia, kehadirannya merupakan kontribusi penting untuk kapasitas penyerapan cahaya di 280 nm. wilayah sebagian besar protein.
Persyaratan harian untuk triptofan berbeda dengan usia. Pada bayi antara 4 dan 6 bulan, kebutuhan rata-rata adalah sekitar 17 mg per kilogram berat badan per hari; pada anak-anak 10 hingga 12 tahun adalah 3,3 mg per kilogram berat badan per hari dan pada orang dewasa adalah 3,5 mg per kilogram berat badan per hari.
Triptofan diserap melalui usus dan merupakan asam amino ketogenik dan glukogenik pada saat yang bersamaan.
Karena merupakan prekursor serotonin, neurotransmitter penting, triptofan harus mencapai sistem saraf pusat (SSP) dan untuk ini harus melintasi sawar darah-otak, yang ada mekanisme transpor aktif yang spesifik.
Struktur
Triptofan memiliki rumus molekul C11H12N2O2 dan asam amino esensial ini memiliki rantai samping aromatik.
Seperti semua asam amino, triptofan memiliki atom karbon yang terikat pada gugus amino (NH2), atom hidrogen (H), gugus karboksil (COOH) dan rantai samping (R) yang dibentuk oleh struktur heterosiklik, gugus indol.
Nama kimianya adalah asam 2-amino-3-indolyl propionat, ia memiliki massa molekul 204,23 g / mol. Kelarutannya pada 20 ° C adalah 1,06 g dalam 100 g air dan memiliki massa jenis 1,34 g / cm3.
Fitur
Pada manusia, triptofan digunakan untuk sintesis protein dan sangat penting untuk pembentukan serotonin (5-hidroksitriptamin), vasokonstriktor kuat, stimulan kontraksi otot polos (terutama di usus kecil) dan neurotransmitter yang mampu menghasilkan stimulasi psikis, memerangi depresi. dan mengatur kecemasan.
Triptofan adalah prekursor dalam sintesis melatonin dan karena itu memiliki implikasi dalam siklus tidur-bangun.
Asam amino tersebut digunakan sebagai prekursor dalam salah satu dari tiga jalur untuk pembentukan kofaktor NAD, kofaktor yang sangat penting yang berpartisipasi dalam berbagai macam reaksi enzimatik yang berkaitan dengan peristiwa oksidasi-reduksi.
Triptofan dan beberapa prekursornya digunakan untuk pembentukan hormon tanaman yang disebut auksin (asam indole-3-asetat). Auksin adalah hormon tanaman yang mengatur pertumbuhan, perkembangan, dan banyak fungsi fisiologis tanaman lainnya .
Biosintesis
Dalam organisme yang mampu mensintesisnya, kerangka karbon triptofan berasal dari fosfoenolpiruvat dan eritrosa-4-fosfat. Ini, pada gilirannya, terbentuk dari perantara siklus Krebs: oksaloasetat.
Fosfoenolpiruvat dan eritrosa-4-fosfat digunakan untuk sintesis korismat dalam jalur enzimatik tujuh langkah. Fosfoenolpiruvat (PEP) adalah produk glikolisis dan eritrosa-4-fosfat dari jalur pentosa fosfat.
Seperti apa rute sintesis corismate?
Langkah pertama dalam sintesis chorismate adalah pengikatan PEP dengan erythrose-4-phosphate untuk membentuk 2-keto-3-deoxy-D-arabino-heptulosonate-7-phosphate (DAHP).
Reaksi ini dikatalisis oleh enzim 2-keto-3-deoxy-D-arabino-heptulosonate-7-phosphate synthase (DAHP sintase), yang dihambat oleh chorismate.
Reaksi kedua melibatkan siklisasi DAHP oleh dehydroquinate synthase, suatu enzim yang membutuhkan kofaktor NAD, yang direduksi selama reaksi ini; sebagai hasilnya 5-dehydroquinate diproduksi.
Langkah ketiga dari rute ini melibatkan eliminasi molekul air dari 5-dehydroquinate, reaksi yang dikatalisis oleh enzim dehydroquinate dehydratase, yang produk akhirnya sesuai dengan 5-dehydro shikimate.
Gugus keto dari molekul ini direduksi menjadi gugus hidroksil dan, sebagai akibatnya, shikimat terbentuk. Enzim yang mengkatalisis reaksi ini adalah shikimate dehydrogenase yang bergantung pada NADPH.
Langkah kelima dari rute melibatkan pembentukan shikimate 5-fosfat dan konsumsi molekul ATP oleh aksi enzim yang dikenal sebagai shikimate kinase, yang bertanggung jawab untuk fosforilasi shikimate pada posisi 5.
Selanjutnya, dari shikimate 5-phosphate dan dengan aksi 3-enolpyruvyl shikimate-5-phosphate synthase, 3-enolpyruvyl shikimate 5-phosphate dihasilkan. Enzim tersebut mendorong perpindahan gugus fosforil dari molekul PEP kedua oleh gugus hidroksil dari karbon pada posisi 5 dari shikimat 5-fosfat.
Reaksi ketujuh dan terakhir dikatalisis oleh chorismate synthase, yang menghilangkan fosfat dari 3-enolpyruvyl shikimate 5-phosphate dan mengubahnya menjadi chorismate.
Dalam jamur N. crassa , kompleks enzim multifungsi tunggal mengkatalisis lima dari tujuh reaksi di jalur ini, dan tiga enzim lain ditambahkan ke kompleks ini yang akhirnya menghasilkan triptofan.
Sintesis triptofan pada bakteri
Pada E. coli, transformasi korismat menjadi triptofan mencakup lima jalur langkah enzimatik tambahan:
Pertama, enzim anthranilate synthase mengubah chorismate menjadi anthranilate. Sebuah molekul glutamin berpartisipasi dalam reaksi ini, yang menyumbangkan gugus amino yang mengikat cincin indol triptofan dan menjadi glutamat.
Langkah kedua dikatalisis oleh anthranilate phosphoribosyl transferase. Dalam reaksi ini, molekul pirofosfat dipindahkan dari 5-fosforibosil-1-pirofosfat (PRPP), suatu metabolit yang kaya energi, dan N- (5′-fosforibosil) -anthranilat terbentuk.
Reaksi ketiga dari rute sintesis triptofan ini melibatkan partisipasi enzim fosforibosil-anthranilat isomerase. Di sini cincin furan dari N- (5′-phosphoribosyl) -anthranilate dibuka dan 1- (o-carboxyphenylamino) -1-deoxyribulose 5-phosphate dibentuk melalui tautomerisasi.
Kemudian indole-3-gliserol fosfat terbentuk, dalam reaksi yang dikatalisis oleh indole-3-gliserol fosfat sintase, di mana molekul CO2 dan H2O dilepaskan dan 1- (o-karboksifenilamino) -1- disikliskan deoksiribulosa 5-fosfat.
Reaksi terakhir dari jalur ini berakhir dengan pembentukan triptofan ketika triptofan sintase mengkatalisis reaksi indole-3-gliserol fosfat dengan satu molekul PLP (piridoksal fosfat) dan satu lagi serin, melepaskan gliseraldehida 3-fosfat dan membentuk triptofan.
Degradasi
Pada mamalia, triptofan didegradasi di hati menjadi asetil-KoA dalam jalur yang melibatkan dua belas langkah enzimatik: delapan untuk mencapai -ketoadipate dan 4 lagi untuk mengubah -ketoadipate menjadi asetil koenzim A.
Urutan degradasi menjadi -ketoadipat adalah:
Triptofan → N- formil kuinurenin → Kuinurenin → 3-hidroksi kuinurenin → 3-hidroksi-anthranilat → -semialdehida 2-amino-3-karboksi mukonat → -semialdehida -amino mukonat → 2-amino mukonat → -ketoadipate.
Enzim yang mengkatalisis reaksi ini masing-masing adalah:
Triptofan 2-3-dioksigenase, kinurenin formamidase, monooksigenase yang bergantung pada NADPH, kinureninase, 3-hidroksi-anthranilate oksigenase, dekarboksilase, -semialdehida -aminonuconic dehydrogenase yang bergantung pada NAD dan -amino muconate reductase yang bergantung pada NADPH.
Setelah -ketoadipate dihasilkan, glutaryl-CoA dibentuk oleh dekarboksilasi oksidatif. Ini, dengan -oksidasi, membentuk Glutaconyl-CoA yang kehilangan atom karbon dalam bentuk bikarbonat (HCO3-), memperoleh molekul air dan berakhir sebagai crotonyl-CoA.
Krotonil-KoA, juga melalui -oksidasi, menghasilkan asetil-KoA. Asetil-KoA tersebut dapat mengikuti beberapa jalur, terutama glukoneogenesis, untuk membentuk glukosa, dan siklus Krebs, untuk membentuk ATP, sesuai kebutuhan.
Namun, molekul ini juga dapat diarahkan pada pembentukan badan keton, yang akhirnya dapat digunakan sebagai sumber energi.
Makanan kaya triptofan
Daging merah pada umumnya, ayam dan ikan (terutama ikan berminyak seperti salmon dan tuna) sangat kaya akan triptofan. Susu dan turunannya, telur, terutama kuning telur, juga merupakan makanan dengan kandungan triptofan yang melimpah.
Makanan lain yang berfungsi sebagai sumber alami asam amino ini adalah:
– Kacang-kacangan seperti walnut, almond, pistachio, dan kacang mete, antara lain.
– Sereal beras.
– Biji-bijian kering seperti kacang, lentil, buncis, kedelai, quinoa, dll.
– Ragi bir dan kacang segar, pisang dan pisang raja, nanas atau nanas, alpukat, plum, selada air, brokoli, bayam, dan cokelat.
Manfaat asupannya
Konsumsi triptofan mutlak diperlukan untuk mensintesis semua protein yang termasuk dalam strukturnya dan melalui fungsinya yang berbeda memungkinkan untuk mengatur suasana hati, siklus tidur dan bangun dan berbagai macam proses biokimia di mana NAD berpartisipasi. .
Selain efeknya yang diketahui pada suasana hati, serotonin (berasal dari triptofan) terlibat dalam berbagai fungsi kognitif yang terkait dengan pembelajaran dan memori, yang oleh karena itu juga terkait dengan triptofan.
Ada data yang menunjukkan hubungan antara suasana hati, serotonin dan sumbu gastrointestinal-otak sebagai sistem pengaruh dua arah antara pusat emosional dan kognitif otak dan fungsi perifer saluran pencernaan.
Penggunaannya sebagai suplemen makanan untuk pengobatan beberapa gangguan, terutama yang berhubungan dengan sistem saraf pusat, telah menjadi sangat kontroversial karena transportasi kompetitifnya dengan asam amino netral yang jauh lebih melimpah membuat sulit untuk mencapai peningkatan triptofan yang signifikan dan berkelanjutan setelahnya. pemberian oral.
Terlepas dari kontroversi ini, penggunaannya sebagai adjuvant telah didalilkan dalam:
– Pengobatan nyeri
– Gangguan tidur
– Pengobatan depresi
– Pengobatan mania
– pengurangan nafsu makan
Gangguan kekurangan
Eliminasi atau defisiensi triptofan sentral dikaitkan dengan depresi, kegagalan perhatian, gangguan memori, gangguan tidur, dan kecemasan.
Pada pasien depresi dan bunuh diri ditemukan perubahan konsentrasi triptofan dalam darah dan cairan serebrospinal . Lebih lanjut, beberapa pasien dengan anoreksia nervosa menunjukkan kadar triptofan serum yang rendah.
Beberapa pasien poliurik, yang kehilangan vitamin B6 dan seng, sering mengalami fobia dan kecemasan dan membaik dengan suplemen makanan yang kaya triptofan.
Sindrom karsinoid ditandai dengan adanya tumor usus kecil yang menyebabkan diare, penyakit pembuluh darah dan bronkokonstriksi dan berhubungan dengan defisiensi niasin dan triptofan.
Pellagra adalah kondisi patologis yang disertai dengan diare, demensia, dermatitis dan dapat menyebabkan kematian, ini juga diobati dengan suplemen niasin dan triptofan.
Penyakit Hartnup ada hubungannya, di antara beberapa hal, dengan gangguan metabolisme beberapa asam amino, termasuk triptofan.
Dalam kasus kekurangan enzim triptofan-2,3-monooksigenase, ini adalah penyakit keturunan resesif yang ditandai dengan keterbelakangan mental dan kelainan kulit seperti pellagra.
Referensi
- Halvorsen, K., & Halvorsen, S. (1963). penyakit Hartnup. Anak , 31 (1), 29-38.
- Hood, SD, Bell, CJ, Argyropoulos, SV, & Nutt, DJ (2016). Jangan panik. Panduan untuk penipisan triptofan dengan provokasi kecemasan khusus gangguan. Jurnal Psikofarmakologi , 30 (11), 1137-1140.
- Jenkins, TA, Nguyen, JC, Polglaze, KE, & Bertrand, PP (2016). Pengaruh triptofan dan serotonin pada suasana hati dan kognisi dengan kemungkinan peran sumbu usus-otak. Nutrisi , 8 (1), 56.
- Kaye, WH, Barbarich, NC, Putnam, K., Gendall, KA, Fernstrom, J., Fernstrom, M.,… & Kishore, A. (2003). Efek ansiolitik dari penipisan triptofan akut pada anoreksia nervosa. Jurnal Internasional Gangguan Makan , 33 (3), 257-267.
- Murray, RK, Granner, DK, Mayes, P., & Rodwell, V. (2009). Biokimia Harper yang diilustrasikan. 28 (hal. 588). New York: McGraw-Hill.
- Nelson, DL, Lehninger, AL, & Cox, MM (2008). Prinsip-prinsip biokimia Lehninger . Macmillan.

