gliseraldehida 3-fosfat (GAP) adalah metabolit dari glikolisis (nama yang berasal dari bahasa Yunani; glicos = manis atau gula; lisis = pecah), yang merupakan jalur metabolisme yang molekul bertobat glukosa menjadi dua molekul piruvat untuk menghasilkan energi dalam bentuk adenosin trifosfat (ATP).
Dalam sel, gliseraldehida 3-fosfat menghubungkan glikolisis dengan glukoneogenesis dan jalur pentosa fosfat. Dalam organisme fotosintesis, gliseraldehida 3-fosfat, yang berasal dari fiksasi karbon dioksida, digunakan untuk biosintesis gula. Di hati, metabolisme fruktosa menghasilkan GAP, yang dimasukkan ke dalam glikolisis.
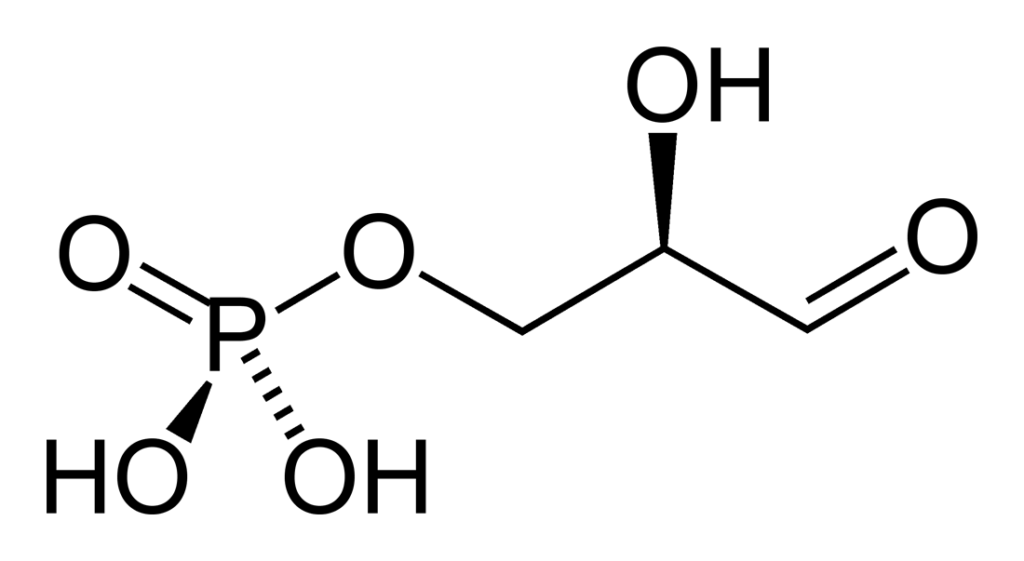
Sumber: Benjah-bmm27 [Domain publik]
Indeks artikel
Struktur
Gliseraldehida 3-fosfat adalah gula terfosforilasi yang memiliki tiga karbon. Rumus empirisnya adalah C 3 H 7 O 6 P. Gugus aldehida (-CHO) adalah karbon 1 (C-1), gugus hidroksimetilen (-CHOH) adalah karbon 2 (C-2) dan gugus hidroksimetil (-CH 2 OH) adalah karbon 3 (C3). Yang terakhir membentuk ikatan dengan gugus fosfat (ikatan fosfoester).
Konfigurasi gliseraldehida 3-fosfat pada kiral C-2 adalah D. Dengan konvensi, sehubungan dengan karbon kiral, dalam proyeksi Fischer gugus aldehida diwakili ke atas, gugus hidroksimetilfosfat ke bawah, gugus hidroksil ke bawah, kanan dan atom hidrogen ke kiri.
Karakteristik
Gliseraldehida 3-fosfat memiliki massa molekul 170,06 g/mol. Perubahan energi bebas Gibbs standar (ΔGº) untuk setiap reaksi harus dihitung dengan menambahkan variasi energi bebas produk, dan mengurangkan jumlah variasi energi bebas reaktan.
Dengan cara ini, variasi energi bebas (ΔGº) pembentukan gliseraldehida 3-fosfat ditentukan, yaitu -1.285 KJ × mol -1 . Berdasarkan kesepakatan, dalam keadaan standar 25 ° C dan 1 atm, energi bebas unsur murni adalah nol.
Fitur
Glikolisis dan glukoneogenesis
Glikolisis hadir di semua sel. Ini dibagi menjadi dua fase: 1) fase investasi energi dan sintesis metabolit dengan potensi transfer gugus fosfat tinggi, seperti gliseraldehida 3-fosfat (GAP); 2) Langkah sintesis ATP dari molekul dengan potensi transfer gugus fosfat tinggi.
Gliseraldehida 3-fosfat dan dihidroksiaseton fosfat terbentuk dari fruktosa 1,6-bifosfat, suatu reaksi yang dikatalisis oleh enzim aldolase. Gliseraldehida 3-fosfat diubah menjadi 1,3-bisfosfogliserat (1,3BPG), melalui reaksi yang dikatalisis oleh enzim GAP dehidrogenase.
GAP dehidrogenase mengkatalisis oksidasi atom karbon aldehida dan mentransfer gugus fosfat. Dengan demikian, anhidrida campuran (1,3BPG) terbentuk di mana gugus asil dan atom fosfor rentan terhadap reaksi serangan nukleofilik.
Selanjutnya, dalam reaksi yang dikatalisis oleh 3-fosfogliserat kinase, 1,3BPG mentransfer gugus fosfat dari karbon 1 ke ADP, membentuk ATP.
Karena reaksi yang dikatalisis oleh aldolase, GAP dehidrogenase dan 3-fosfogliserat kinase berada dalam kesetimbangan (ΔGº ~ 0), mereka reversibel, oleh karena itu menjadi bagian dari jalur glukoneogenesis (atau sintesis glukosa baru). ).
Jalur pentosa fosfat dan siklus Calvin
Dalam jalur pentosa fosfat, gliseraldehida 3-fosfat (GAP) dan fruktosa 6-fosfat (F6P) dibentuk dengan memotong reaksi dan pembentukan ikatan CC, dari pentosa, xilulosa 5-fosfat dan ribosa 5-fosfat.
Gliseraldehida 3-fosfat dapat mengikuti jalur glukoneogenesis dan membentuk glukosa 6-fosfat, yang melanjutkan jalur pentosa fosfat. Glukosa dapat sepenuhnya dioksidasi menghasilkan enam CO 2 molekul melalui langkah oksidatif dari jalur pentosa fosfat.
Pada siklus Calvin, CO 2 adalah tetap sebagai 3-fosfogliserat, dalam reaksi dikatalisis oleh karboksilase bifosfat ribulosa. 3-fosfogliserat kemudian direduksi oleh NADH melalui aksi enzim yang disebut GAP dehidrogenase.
2 Molekul GAP diperlukan untuk biosintesis heksosa, seperti glukosa, yang digunakan untuk biosintesis pati atau selulosa pada tanaman .
Metabolisme fruktosa
Enzim fruktokinase mengkatalisis fosforilasi fruktosa oleh ATP pada C-1, membentuk fruktosa 1-fosfat. Aldolase A, ditemukan di otot, spesifik untuk fruktosa 1,6-bifosfat sebagai substrat. Aldolase B ditemukan di hati dan spesifik untuk fruktosa 1-fosfat sebagai substrat.
Aldolase B mengkatalisis pemecahan aldol fruktosa 1-fosfat dan menghasilkan dihidroksiaseton fosfat dan gliseraldehida. Gliseraldehida kinase mengkatalisis fosforilasi gliseraldehida oleh ATP, membentuk zat antara glikolitik, gliseraldehida 3-fosfat (GAP).
Dengan cara yang berbeda, gliseraldehida diubah menjadi gliserol oleh alkohol dehidrogenase yang menggunakan NADH sebagai substrat donor elektron. Gliserol kinase kemudian memfosforilasi gliserol melalui ATP, membentuk gliserol fosfat. Metabolit yang terakhir direoksidasi, membentuk dihidroksiaseton fosfat (DHAP) dan NADH.
DHAP diubah menjadi GAP oleh enzim triose phosphate isomerase. Dengan cara ini, fruktosa diubah menjadi metabolit glikolisis. Namun, fruktosa yang diberikan secara intravena dapat menyebabkan kerusakan serius, terdiri dari penurunan drastis fosfat dan ATP intraseluler. Asidosis laktat bahkan terjadi.
Kerusakan fruktosa disebabkan oleh fakta bahwa fruktosa tidak memiliki titik setel yang biasanya dimiliki katabolisme glukosa. Pertama, fruktosa memasuki otot melalui GLUT5, yang tidak tergantung pada insulin.
Kedua, fruktosa secara langsung diubah menjadi GAP dan dengan demikian melewati regulasi enzim phosphofruct kinase (PFK) pada awal glikolisis.
Melalui Entner-Doudoroff
Glikolisis adalah jalur universal untuk katabolisme glukosa. Namun, beberapa bakteri alternatif menggunakan jalur Entner-Doudoroff. Jalur ini melibatkan enam langkah yang dikatalisis oleh enzim, di mana glukosa diubah menjadi GAP dan piruvat, yang merupakan dua produk akhir dari jalur ini.
GAP dan piruvat diubah menjadi etanol melalui reaksi fermentasi alkohol.
Referensi
- Berg, JM, Tymoczco, JL, Stryer, L. 2015. Biokimia. Kursus singkat. WH Freeman, New York.
- Miesfeld, RL, McEvoy, MM 2017. Biokimia. WW Norton, New York.
- Nelson, DL, Cox, MM 2017. Prinsip-prinsip biokimia Lehninger. WH Freeman, New York.
- Salway JG 2004. Metabolisme sekilas. Blackwell, Malden.
- Voet, D., Voet, JG, Pratt, CW 2008. Dasar-dasar biokimia: kehidupan di tingkat molekuler. Wiley, Hoboken.

